Первый анализ результатов обследования — при распределении больных только по величине ОФВ1 (см. таблицу) — демонстрирует нам любопытный факт: прогрессирование бронхиальной обструкции проявляется, с одной стороны, снижением ОФВ1, а с другой — повышением ответа на беротек, что, по-видимому, связано с увеличением выраженности бронхоспазма по мере увеличения длительности заболевания. В общей массе обследованных не выявлено значимого положительного или отрицательного ответа на адреналин, однако, очевидна тенденция к появлению отрицательной реакции на этот фармакологический агент. В то же время достоверно установлено, что, несмотря на повышение ответа на беротек, обратимость бронхиальной обструкции снижается. Если в первые 8–9 лет заболевания нарушение проходимости дыхательных путей обратимо этим бронхорасширяющим препаратом в среднем на 82–100%, то в последующие годы этот показатель падает до 55–68%. Уменьшение обратимости бронхиальной обструкции нельзя объяснить появлением отрицательного ответа на адреналин, поскольку его величина не превышает в среднем -3%. По-видимому, в основе неполной обратимости обструкции лежат нарушения экспекторации. Это подтверждается наличием прямой корреляционной зависимости (r=0,436, p<0,01) между величиной Texp и длительностью заболевания.
Таким образом, можно утверждать, что прогрессирование бронхиальной обструкции при астме характеризуется повышением степени бронхоспазма, появлением слабой бронхоконстрикции на адреналин и усугублением нарушений экспекторации. Это утверждение совпадает с существующими представлениями об эволюции астмы (de Montis G. Neue Wege in der Asthmatherapie. Therapiewoche 1985; 35: 4121–4122) и данными о том, что коэффициент восстановления ОФВ1 до должных величин на ингаляцию бронхорасширяющих препаратов при проведении фармакологического тестирования коррелирует с выживаемостью больных (Brown R.D., Grattan G. Reversibility of airflow obstruction. Lancet. 1988; 1: 586–587).
Несколько иная картина выявляется при распределении пациентов не только по величине ОФВ1, но и по ответу на адреналин (см. таблицу). Выясняется, что по мере увеличения длительности заболевания, больные совершенно различно реагируют на адреналин: положительным или отрицательным ответом, а в ряде случаев — отсутствием такового. Возникает закономерный вопрос: следствием какого эффекта — альфа- или бета-стимулирующего — является бронходилатирующее или бронхоконстрикторное действие адреналина на фоне предшествующей ингаляции беротека? Данные повторного тестирования 51 пациента 6-й и 7-й групп с противоотечным альфа-адреномиметиком нафтизином дают основание утверждать, что эти эффекты адреналина обусловлены его альфа-стимулирующим действием. Это подтверждается и данными другой таблицы при отсутствии достоверного ответа на селективный бета-2-агонист — беротек — ингаляция адреналина вызывает в одном случае бронходилатацию, а в другом — бронхоконстрикцию, что очевидно является результатом стимуляции альфа-рецепторов.
Положительный ответ бронхов на адреналин, как следствие уменьшения воспалительного отека слизистой бронхов, несомненно является реакцией благоприятной, так как способствует улучшению функции внешнего дыхания. В этой связи становится понятным, почему в целом ряде случаев эффективность адреналина и беротека при снятии приступов удушья одинакова (Naspitz C.K., Sole D., Wandalsen N. Treatment of acute attacks of bronchial asthma. A comparative study of epi-nephrine (subcutaneous) and fenoterol (inhalation). Ann. Allergy 1987; 59: 21–24).
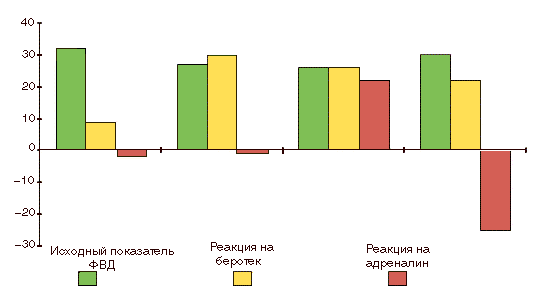
Рис. Реакция бронхиального дерева на беротек и адреналин (в 4-7 группах обследованных):
исх ФВД% — исходные показатели (МОС25-75); % бер и % адр — изменение показателя в % после ингаляции беротека и адреналина соответственно
Это наблюдается в тех случаях, когда в группе обследуемых нет пациентов со стимулированным адреналином отрицательным ответом бронхов. В этих случаях адреналин, оказывающий также и бета-2-стимулирующее действие, является не менее эффективным, чем беротек (5-я группа). Если же при этом адреналин, вследствие альфа-стимуляции, дополнительно вызывает противоотечное положительное действие, то его эффективность для снятия астматических приступов может быть даже выше, чем у беротека (6-я группа).
Что касается альфа-стимулированной бронхоконстрикции, то механизм ее возникновения нельзя объяснить только слабым сокращением мышц бронхов вследствие стимуляции альфа-рецепторов (Парсонс Г.Х. Лечение бронхиальной астмы у взрослых. В кн.: Бронхиальная астма. Принципы диагностики и лечения. Под ред. М.Э. Гершвина. Пер. с англ. М.: Медицина, 1984, с. 355–381), поскольку, как видно из рисунка, отрицательный ответ на адреналин не только равен по величине бронхорасширяющему эффекту беротека, но даже превышает его (7-я группа).
Каков же механизм развития альфа-стимулированной бронхоконстрикции? Для ответа на этот вопрос необходимо проанализировать результаты обследования больных 4, 6, и 7-й групп до и после лечения. Чем различались исходно пациенты 6-й и 7-й групп? Только ответом на адреналин. В 6-й группе бронхиальный ответ на адреналин после ингаляции беротека положительный, а в 7-й — отрицательный.
После курса проведенного лечения в 7-й группе альфа-стимулированная бронхоконстрикция, проявляющаяся снижением МОС25-75, сохраняется только у субъектов, получавших лечение по обычной схеме. У пациентов, получавших лечение по ингаляционной схеме, альфа-стимулированная бронхоконстрикция исчезает. Различие в результатах лечения по обычной и ингаляционной схемам наблюдается также в 4-й группе больных. Как видно из данных, после курса проведенного лечения у них выявляется значимый ответ на беротек (превышающий в среднем 10% от должных значений). В то же время у субъектов, получавших лечение по обычной схеме (только с пероральными экспекторантами), появляется альфа-стимулированная бронхоконстрикция (в ответ на ингаляцию адреналина достоверно снижается показатель МОС25-75). У пациентов, получавших лечение с ингаляционными экспекторантами, альфа-стимулированной бронхоконстрикции не выявляется. Чем же отличаются пациенты 4-й группы от остальных субъектов? Исходное обследование выявило, что у них были наиболее выраженные нарушения экспекторации: Texp превышало в среднем 48 ч (см. таблицу).
Как было показано выше, подобные нарушения экспекторации относятся ко II степени и не могут быть полностью ликвидированы пероральными отхаркивающими средствами. Эффективная коррекция этих нарушений может быть достигнута назначением только ингаляционной отхаркивающей терапии.
Из всего сказанного можно сделать единственный вывод: основой возникновения альфа-стимулированной бронхоконстрикции является неполная коррекция нарушений экспекторации. Это подтверждается и клиническими наблюдениями в процессе исходного обследования: у многих пациентов 6-й и 7-й групп после ингаляции адреналина появлялись кашель и желание откашляться. Однако эффективная экспекторация отмечалась только у субъектов 6-й группы. В 7-й группе попытки откашлять мокроту были неэффективными и приводили в последующем к появлению затрудненного дыхания или приступа удушья. Эти наблюдения обусловлены своеобразной цепочкой последовательно развивающихся механизмов, схематически представленной на рисунке.
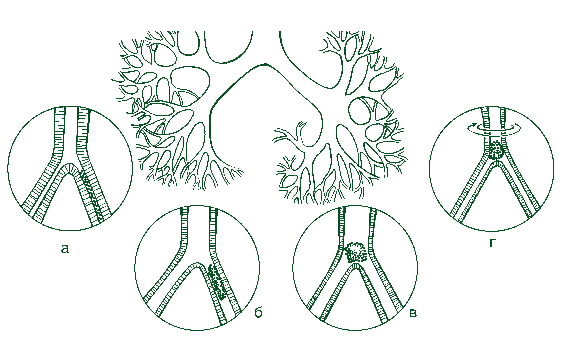
Рис. Механизм развития альфа-стимулированной бронхоконстрикции
Выраженный воспалительный отек слизистой в дистальном отделе респираторного тракта препятствует эвакуации слизистых пробок из периферических бронхов (а) — возникает ситуация, аналогичная так называемому «запертому легкому» («locked lung»). Ингаляция противоотечного препарата с альфа-стимулирующим эффектом (адреналина или нафтизина) снимает отек, и при этом повышение скорости воздушного потока в этих бронхах способствует продвижению слизистых пробок от более мелких бронхов к более крупным (б). Пациенты с незначительным количеством слизи благополучно откашливаются, а в случае отсутствия слизи в этих отделах дыхательных путей снятие отека слизистой улучшает вентиляцию без эффекта откашливания (6-я группа).
Совершенно другой эффект наблюдается в случае достаточно большого количества слизистых пробок в периферических воздухопроводящих путях. Их движение перекрывает просвет дыхательных путей в месте дихотомического деления бронхов (в). При этом непродуктивный кашель и рефлекторный спазм, как следствие раздражения холинергических рецепторов, приводит к полной обтурации бронха (г) и еще большим нарушениям проходимости дыхательных путей (7-я группа).
В случае преобладания рефлекторного бронхоспазма и незначительной обтурации, альфа-стимулированная бронхоконстрикция полностью обратима холинолитиками. В случае выраженной обтурации последующая ингаляция холинолитика абсолютно неэффективна. Таким образом, противоотечный эффект препаратов с альфа-стимулирующим действием вызывает в одном случае бронходилатацию, а в другом — бронхоконстрикцию.
Известно, что альфа-рецепторы по своей природе делятся на два подтипа: альфа-1 и альфа-2. Альфа-1-рецепторы локализуются в постсинаптических мембранах (в сосудах и гладкой муску-латуре дистальных бронхов, вероятно ими и обусловлена слабая альфа-стимулированная бронхоконстрикция). Альфа-2-рецепторы расположены внесинаптически в стенке сосудов (в рамках этого обсуждения не рассматриваются пре- и постсинаптические альфа-2-рецепторы в ЦНС). Противоотечное действие альфа-стимуляторов реализуется, во-первых, непосредственным альфа-1-постсинаптическим действием в микрососудах слизистой бронхов, во-вторых, непосредственным альфа-2-внесинаптическим действием в сосудах, а также альфа-2-стимуляцией, приводящей к высвобождению норадреналина, оказывающего преимущественно альфа-1-стимулирующее действие. Более подробно на этом достаточно сложном вопросе останавливаться в рамках данного исследования нет смысла. Ибо в случае с бронхиальным деревом альфа-адреностимуляция приводит преимущественно к противоотечному эффекту в результате сужения сосудов слизистой оболочки бронхов.
Поскольку основным механизмом противоотечного действия адреналина является сужение сосудов микроциркуляторного русла и уменьшение их проницаемости, то можно уверенно утверждать, что выраженная бронхоконстрикторная реакция после ингаляции адреналина развивается вследствие стимуляции альфа-рецепторов сосудов слизистой и уменьшения ее отека с последующим перемещением слизистых пробок из периферических бронхов, а не стимуляцией альфа-рецепторов гладкой мускулатуры. Если бы возникновение альфа-стимулированной бронхоконстрикции было вызвано стимуляцией альфа-рецепторов бронхиальной мускулатуры, то назначение отхаркивающей терапии по различным схемам (пероральной или ингаляционной) не оказывало бы существенного влияния на эту реакцию. Данное объяснение механизма развития альфа-стимулированной бронхоконстрикции хорошо согласуется, во-первых, с предположением о постоянстве противоотечного эффекта адреналина, во-вторых, с давно существующим мнением о том, что в обструкции периферических бронхов преобладающим механизмом является не спазм, а отек слизистой с обтурацией их слизистыми пробками, и, в-третьих, с имеющимися в клинической практике случаями ухудшения состояния пациентов после введения им адреналина (Парсонс Г.Х. Лечение бронхиальной астмы у взрослых. В кн.: Бронхиальная астма. Принципы диагностики и лечения. Под ред. М.Э. Гершвина. Пер. с англ. М.: Медицина, 1984, с. 355–381).
Что касается слабой альфа-стимулированной бронхоконстрикции, то, поскольку она обратима холинолитиками, ее следует считать рефлекторной. Эта реакция в силу рефлекторного механизма возникновения может быть обусловлена не только механическим (движение слизистых пробок), но и физическим (осмотическим) или химическим (изменение pH) воздействием ингалируемых альфа-стимуляторов на слизистую бронхов, что подтверждается и данными литературы (Snashall P.D., Boother F.A., Sterling G.M. The effect of alpha-adrenoreceptor stimulation on the airways of normal and asthmatic man. Clin. Sci. Mol. Med. 1978; 54: 283–289), хотя они в достаточной мере противоречивы.
Детальный анализ степени выраженности и времени появления альфа-стимулированной бронхоконстрикции в зависимости от индивидуальных особенностей пациентов также выявляет любопытные закономерности.
Зависимость величины альфа-стимулированной бронхоконстрикции от пола субъектов проявляется тем, что у женщин она достоверно выше, несмотря на то, что средняя длительность заболевания у них меньше. При этом соотношение женщин и мужчин с бронхоконстрикцией на адреналин составляет 3:1, что превышает этот показатель во всей обследованной популяции — 2,35:1. Вероятно, это объясняется противоположным влиянием женских и мужских половых гормонов на эволюцию астмы: эстрогены оказывают отрицательное, а андрогены — положительное действие. Это подтверждается и наличием прямой корреляционной зависимости между степенью бронхоконстрикции и возрастом мужчин, поскольку в процессе старения, как известно, активность андрогенов снижается. По-видимому, нередкие случаи ухудшения течения астмы на фоне дисгормональных изменений у женщин, в частности при беременности (Хэнсон Ф.В. Бронхиальная астма и беременность. В кн.: Бронхиальная астма. Принципы диагностики и лечения. Под ред. М.Э. Гершвина. Пер. с англ. М.: Медицина, 1984, с. 403–410), связаны с увеличением частоты бронхоконстрикторных реакций. Наиболее вероятно, что именно различная специфика действия мужских и женских половых гормонов обусловливает более высокую заболеваемость женщин в возрастной период от 10 до 60 лет (Файф Д., Спейзер Ф.Е. Эпидемиология бронхиальной астмы. В кн.: Бронхиальная астма. Принципы диагностики и лечения. Под ред. М.Э. Гершвина. Пер. с англ. М.: Медицина, 1984, с. 15–25). Любопытно и другое наблюдение: появление альфа-стимулированной бронхоконстрикции не зависит от того, получают пациенты стероиды или нет. Как видно из приведенных данных, в группе субъектов, получающих стероиды, средняя величина отрицательного ответа на адреналин в 1,5 раза выше, чем у не получающих постоянно эти препараты. При этом длительность заболевания у лиц, не получающих стероиды, достоверно меньше. Это, вероятно, объясняется тем, что возникновение отрицательного ответа на адреналин является закономерным этапом в эволюции бронхиальной обструкции, несмотря на то, что стероиды, снимающие отек и воспаление, замедляют ее прогрессирование (Heide D. Moderne Dosier-aerosole in der Behandlung obstruktiver Atemtrakterkrankungen. 3. Inhalierbare Kortikoide. Zarztl. Fortbild. 1984; 78: 49–51) и сегодня наконец признаны «базисными препаратами».
Парадоксальным кажется и другой факт: величина альфа-стимулированной бронхоконстрикции в группе курильщиков значительно меньше, чем в группе некурящих и бывших курильщиков. Понятно, что этот эффект связан с действием никотина как Н-холиномиметика, высвобождающего из мозгового слоя надпочечников депонированный в них эндогенный адреналин, снимающий отек слизистой оболочки бронха. Это подтверждается выявлением обратной корреляции между количеством выкуриваемых сигарет в день и степенью бронхоконстрикции на адреналин.
Что же касается бывших курильщиков, то, по-видимому, прекращение постоянного воздействия высвобождаемого никотином адреналина в сочетании с хроническими воспалительными изменениями слизистой периферических бронхов от длительного воздействия сигаретного дыма являются факторами, усиливающими альфа-стимулированную бронхоконстрикцию. Это подтверждается, наоборот, наличием прямой корреляцией между степенью бронхоконстрикции на адреналин и длительностью курения у этих субъектов. Если считать эти объяснения логичными, то практическая сторона вопроса о курении астматика очевидна:
- НЕОБХОДИМО НАСТАИВАТЬ НА ПРЕКРАЩЕНИИ КУРЕНИЯ БОЛЬНЫХ АСТМОЙ;
- В ТО ЖЕ ВРЕМЯ ОНО ДОЛЖНО СОПРОВОЖДАТЬСЯ ВРАЧЕБНЫМ КОНТРОЛЕМ И ВНЕСЕНИЕМ КОРРЕКТИВ В ПРОВОДИМОЕ ЛЕЧЕНИЕ, ДО ИСЧЕЗНОВЕНИЯ ОТРИЦАТЕЛЬНОГО ОТВЕТА НА АДРЕНАЛИН.
Более высокая степень альфа-стимулированной бронхоконстрикции у пациентов с непереносимостью НСПП объясняется, вероятно, свойством аспирина и его аналогов вызывать не только спазм бронхиальной мускулатуры (Стюарт С.Р., Гершвин М.Э. Непереносимость ацетилсалициловой кислоты (аспирина) и бронхиальная астма. В кн.: Бронхиальная астма. Принципы диагностики и лечения. Под ред. М.Э. Гершвина. Пер. с англ. М.: Медицина, 1984, с. 210–224), но и набухание слизистых оболочек в результате расширения капилляров или повышения их проницаемости. Данные литературы свидетельствуют, что даже у здоровых субъектов аспирин повышает назальное сопротивление (Jones A.S., Lancer J.M., Moir A., Stevens J.C.: Effect of aspirin on nasal resistance to airflow. Brit. Med. J., 1985; 290: 1171–1173), что можно объяснить только набуханием слизистой носа в результате ее отека.
Особенно неблагоприятным фактором, определяющим выраженность и сроки появления альфа-стимулированной бронхоконстрикции, является инфекционно-воспалительный процесс, вызываемый персистирующей в дыхательных путях микробной флорой. Как видно из приведенных данных, альфа-стимулированная бронхоконстрикция возникает значительно раньше и выраженность ее значительно больше в случае присоединения грамотрицательной микробной флоры, в частности бактерий E. Coli, вызывающих, по-видимому, более выраженное воспаление, чем грамположительная инфекция. В этой связи становится понятной необходимость назначения в ряде случаев высокоэффективных антибактериальных средств.
В такой же мере неблагоприятным фактором, усугубляющим степень выраженности альфа-стимулированной бронхоконстрикции, является высокий уровень иммуноглобулинов класса E, определяющих Ig E-зависимое высвобождение целого ряда воспалительных медиаторов из тучных клеток (Вассерман С.И. Патофизиология медиаторов при бронхиальной астме. В кн.: Бронхиальная астма. Принципы диагностики и лечения. Под ред. М.Э. Гершвина. Пер. с англ. М.: Медицина, 1984, с. 48–69), которые вызывают воспаление и отек слизистой, обусловленный повышением капиллярной проницаемости. Эти же медиаторы способствуют и повышенному образованию секрета в периферических бронхах, усугубляющего обструкцию (Casale T.B., Marom Z. Mast cells and asthma. The role of mast cell mediators in the pathogenesis of allergic asthma. Ann. Allergy 1983; 51: I: 2–6).
Итак, подводя итоги вышесказанному, можно утверждать, что эволюция обструкции дыхательных путей у больных астмой проявляется изменением бронхиального ответа на адреналин.
Начало первого этапа болезни проявляется появлением первой «волны» воспаления и положительной реакцией на адреналин: у субъектов 1-й группы его действие связано с уменьшением отека слизистой бронхиального дерева, что подтверждает имеющиеся данные о ключевой роли воспаления в возникновении и прогрессировании астмы в докладе «International consensus report…» и некоторых более ранних публикациях (Reed C.E. New therapeutic approaches in asthma. J. Allergy Clin. Immunol. 1986; 77: 537–543). Затем появляются пациенты с бронхоконстрикторной реакцией на адреналин (2-я группа), что свидетельствует об одновременном наличии воспалительного отека и начальных нарушений экспекторации в периферических бронхах, которые сохраняются у больных астмой даже в фазе ремиссии (Уоннер А. Морфология обструктивных процессов в воздухоносных путях. В кн.: Бронхиальная астма. Принципы диагностики и лечения. Под ред. М.Э. Гершвина. Пер. с англ. М.: Медицина, 1984, с. 105–116).
Одновременно в этих группах выявляется положительный ответ на беротек, величина которого существенно превышает эффект снятия физиологического тонуса гладкой мускулатуры у здоровых лиц (Солопов В.Н., Луничкина И.В., 1990). Однако прирост более 10% от должных значений выявляется только по показателю МОС25-75, так как величина ОФВ1 практически нормальна. Дальнейшее прогрессирование заболевания связано с формированием выраженного бронхоспазма (3-я группа). При этом частота бронходилатирующего и бронхоконстрикторного эффектов адреналина во всей группе в целом, вероятно, одинакова, что проявляется отсутствием достоверного ответа на этот фармакологический агент.
Последующая эволюция бронхиальной обструкции (в среднем через 10 лет от начала заболевания), по всей вероятности, идет двумя путями: в одном случае прогрессируют нарушения экспекторации (4-я группа), в другом — усиление спазма бронхов (5-я группа), что приводит к значительному снижению всех показателей ФВД: ОФВ1 и МОС25-75. При этом в обеих группах отсутствует достоверный ответ на адреналин. Различаются они только по ответу на бета-2-агонисты: в 4-й группе отсутствует значимый ответ на беротек, что, вероятно, связано с обтурацией просвета бронхов слизистыми пробками вследствие выраженных нарушений экспекторации (Кэннер Р.Э., Ватанабе С. Значение исследования легочной функции у больных бронхиальной астмой. В кн.: Бронхиальная астма. Принципы диагностики и лечения. Под ред. М.Э. Гершвина. Пер. с англ. М.: Медицина, 1984, с. 128–130).
В 5-й группе, наоборот, величина ответа на беротек максимальна, а нарушения экспекторации — минимальны. Преобладание бронхоспазма или обтурации, по-видимому, обусловлено как особенностями развития заболевания у каждого конкретного пациента, так и различиями в проводимом лечении.
Следующий этап эволюции обструктивного синдрома при астме связан с развитием второй «волны» воспаления и появлением положительного ответа на адреналин в 6-й группе. При этом ответ на беротек по сравнению с 5-й группой снижается, а нарушения экспекторации усиливаются. В дальнейшем прогрессирование воспаления в сочетании с нарушениями экспекторации приводит к возникновению ситуации, при которой появляется бронхоконстрикторный ответ на адреналин, и он превышает бронхорасширяющее действие беротека (7-я группа). На этом этапе, по-видимому, ситуация начинает выходить из-под контроля.
С учетом этих данных становятся понятными случаи так называемой «нестабильной» или «эмоциональной», а в отечественной интерпретации — «нервно-психической» астмы (Парсонс Г.Х. Лечение бронхиальной астмы у взрослых. В кн.: Бронхиальная астма. Принципы диагностики и лечения. Под ред. М.Э. Гершвина. Пер. с англ. М.: Медицина, 1984, с. 355–381). Она проявляется высвобождением большого количества эндогенного адреналина (или норадреналина) вследствие стресса или эмоциональной нестабильности на фоне чрезмерного употребления бета-симпатомиметиков, вызывая альфа-стимулированную бронхоконстрикцию с возникновением приступов удушья и затрудненного дыхания. Именно среди пациентов эмоционально неустойчивых, несмотря на лечение стероидами, отмечаются случаи внезапной смерти (Picado C., Montserrat J.M., Pablo J., Augusti-Vival A. Predis-posing factor to death after recovery from a life-threatening asthmatic attack. J. Asthma., 1989; 26: 231–236). Попытаемся в этой связи осветить историю проблемы этого феномена и объяснить предложенную еще в 1992 г. теорию внезапной смерти от астмы (Солопов В.Н., 1992, 1994, 1999).
Первая волна внезапных смертей от астмы прокатилась по странам Западной Европы в 50–60-х гг., в частности по Великобритании, когда молодых людей находили мертвыми с зажатыми в руках баллончиками с синтетическими бронхорасширяющими аэрозолями, впервые появившимися тогда на фармацевтическом рынке. Объяснение этих трагических финалов многие исследователи нашли в несовершенстве самих препаратов: недостаточной селективности (избирательности действия) производных адреналина, в их побочном кардиотоксическом действии, а также в так называемом эффекте блокады бронхорасширяющих бета-2-рецепторов продуктами метаболизма этих лекарств.
Но и с появлением высокоселективных бронхорасширяющих аэрозолей случаи внезапной смерти продолжают регистрироваться с фатальной неизбежностью. Более того, случаи внезапной смерти регистрируются и среди лиц, принимавших таблетированные и ингаляционные стероиды. Неприятная сторона этой проблемы заключается в непредсказуемости ситуации: даже удовлетворительно чувствующий себя астматик, принимающий стероиды, не застрахован от внезапной смерти. Для многих исследователей ситуация оказалась тупиковой, а немецкие врачи охарактеризовали ее как «вызов, бросаемый астмой».
В этой связи и родилась следующая гипотеза: ПОВЫШЕНИЕ ЧАСТОТЫ ВНЕЗАПНЫХ СМЕРТЕЙ ОТ АСТМЫ СВЯЗАНО, ВО-ПЕРВЫХ, С ИСПОЛЬЗОВАНИЕМ ДЛЯ ЛЕЧЕНИЯ СИНТЕТИЧЕСКИХ БРОНХОРАСШИРЯЮЩИХ СРЕДСТВ И, ВО-ВТОРЫХ, С ЭВОЛЮЦИЕЙ САМОЙ БОЛЕЗНИ НА ФОНЕ ИЗМЕНИВШИХСЯ УСЛОВИЙ ЖИЗНИ. Логический анализ известных научных фактов позволяет представить их в следующей последовательности:
1. С начала XX века, практически сразу после открытия, выделения и синтеза адреналина, началось его широкое применение для лечения астмы. Он оказался самым эффективным и безопасным из существующих в то время средств: описаны случаи, когда больным для снятия приступов астмы делалось несколько десятков инъекций адреналина в сутки. В то же время на фоне широкого использования адреналина не наблюдалось повышения смертности от астмы, хотя его применение в виде инъекций вызывало ряд побочных эффектов.
Хорошо известно, что адреналин при инъекционном введении, помимо бронхорасширяющего и противоотечного действия, вызывает выраженное сердцебиение и повышение артериального давления. Стремление специалистов устранить побочные эффекты адреналина и определило тактику дальнейших фармакологических исследований: создание препаратов с избирательным бронхорасширяющим действием.
2. В 30–40-х гг. нашего столетия появились первые синтетические бронхорасширяющие вещества: изопропилнорадреналин и орципреналин. И именно с конца 30–40-х гг. стали описываться смертельные исходы или ухудшения состояния астматиков после введения им адреналина на фоне предшествующих ингаляций его синтетических аналогов.
3. А уже в 50–60-х гг. на фоне широкого применения синтетических бронхорасширяющих препаратов стали регистрироваться эпидемии внезапных смертей от астмы. Как уже говорилось, исследователи увидели причину несчастных случаев в несовершенстве бронхорасширяющих препаратов. Однако синтез высокоселективных противоастматических средств (из наиболее известных можно назвать сальбутамол и беротек) не решил проблемы внезапной смерти от астмы.
4. В то же время сформировалась концепция о функциональной недостаточности симпатоадреналовой системы больных астмой, что стимулировало ее активное изучение. Однако при этом оказалось, что содержание эндогенных катехоламинов (адреналина и норадреналина) в крови тяжелых больных превышает физиологическую норму в 5–10 раз, а тяжесть состояния пациентов прямо коррелирует с их концентрацией. Гипотеза о недостаточности адреналина была опровергнута, но никто не предположил при этом, что причиной тяжелого состояния или внезапной смерти может быть повышенная концентрация собственных катехоламинов. Этого не произошло, по-видимому, по той причине, что только 15–20 лет спустя был выявлен следующий научный факт.
5. Случаи внезапной смерти от астмы отмечаются среди лиц эмоционально неустойчивых (то есть потенциально реагирующих на стрессовые ситуации большим выбросом эндогенных катехоламинов).
Объяснить эти факты можно только следующим образом: ВНЕЗАПНАЯ СМЕРТЬ ОТ АСТМЫ ВЫЗЫВАЕТСЯ НЕ ПРИМЕНЕНИЕМ ОТДЕЛЬНО ВЗЯТЫХ БРОНХОРАСШИРЯЮЩИХ СРЕДСТВ, А ИХ ВЗАИМОДЕЙСТВИЕМ С АДРЕНАЛИНОМ В ОРГАНИЗМЕ БОЛЬНОГО. ЭТО ОБУСЛОВЛЕНО ТЕМ, ЧТО БОЛЬНОМУ СИСТЕМАТИЧЕСКИ ВВОДЯТСЯ СИНТЕТИЧЕСКИЕ АНАЛОГИ АДРЕНАЛИНА (И НОРАДРЕНАЛИНА), ИЗБЫТОК КОТОРЫХ ПОСТОЯННО ЦИРКУЛИРУЕТ У НЕГО В КРОВИ.
ПОЭТОМУ РАНО ИЛИ ПОЗДНО МЕЖДУ ИСКУССТВЕННЫМИ И ЕСТЕСТВЕННЫМИ АДРЕНОПОДОБНЫМИ ВЕЩЕСТВАМИ ДОЛЖЕН НЕМИНУЕМО ВОЗНИКНУТЬ КОНФЛИКТ. ЭТОТ КОНФЛИКТ И ПРОЯВЛЯЕТСЯ ФЕНОМЕНОМ ВНЕЗАПНОЙ СМЕРТИ!
Результаты последовательного фармакологического тестирования с беротеком и адреналином, приводящие к возникновению альфа-стимулированной бронхоконстрикции, являются подтверждением этого тезиса.
ТАКИМ ОБРАЗОМ, ПРОВЕДЕННОЕ ИССЛЕДОВАНИЕ ПОЗВОЛЯЕТ УТВЕРЖДАТЬ, ЧТО В РЯДЕ СЛУЧАЕВ ПРИЧИНОЙ ВНЕЗАПНОЙ СМЕРТИ БОЛЬНЫХ АСТМОЙ ЯВЛЯЕТСЯ АЛЬФА-СТИМУЛИРОВАННАЯ БРОНХОКОНСТРИКЦИЯ ПРИ ВЫБРОСЕ В КРОВЬ БОЛЬШОГО КОЛИЧЕСТВА ЭНДОГЕННЫХ КАТЕХОЛАМИНОВ НА ФОНЕ ПРЕДШЕСТВУЮЩИХ ИНГАЛЯЦИЙ СИНТЕТИЧЕСКИХ БЕТА-АДРЕНОМИМЕТИКОВ.
Это подтверждается и данными об их уровне в крови больных астмой (Катаев К.В. Сопоставление содержания адреналина, норадреналина и сульфгидрильных групп в плазме крови с некоторыми общеклиническими и функциональными показателями у больных бронхиальной астмой. Тер. архив, 1976, № 2, с. 100–103): в фазе обострения заболевания концентрация адреналина и норадреналина в плазме превышает нормальную в 5–8 раз. Причем уровень катехоламинов прямо пропорционален тяжести заболевания.
В этой связи становятся понятными и описываемые с начала 40-х гг. случаи смерти больных после инъекций адреналина на фоне предшествующих ингаляций бета-симпатомиметиков или без них (Юренев П.Н., Семенович Н.И., Чучалин А.Г. О причинах смерти у больных бронхиальной астмой. Клин. мед. 1974, № 12, с. 102–109).
Таким образом, выявляется определенная закономерность в прогрессировании бронхиальной обструкции у больных астмой по мере увеличения длительности заболевания: на фоне снижения показателей ФВД появляется последовательно две положительных и две отрицательных «волны» ответа на адреналин, причем бронхоконстрикторный эффект адреналина превышает бронходилатирующий.
Данные по длительности заболевания из подтверждают тот факт, что эволюция бронхиальной обструкции проявляется в дебюте «волной» альфа-стимулированной бронходилатации, а в финале — альфа-стимулированной бронхоконстрикции.
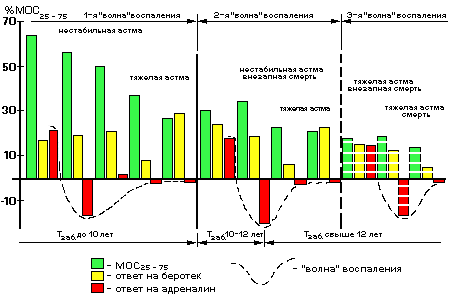
Рис. Эволюция бронхиальной обструкции у больных астмой
Тот факт, что совершенно противоположный ответ на адреналин определяется не индивидуальными особенностями пациентов, а эволюцией астмы, подтверждается и достаточно однородным составом пациентов всех групп. Это не означает, что индивидуальные особенности больных не оказывают влияния на прогрессирование бронхиальной обструкции при астме. Наоборот, индивидуальные особенности каждого субъекта определяют ТЕМПЫ прогрессирования обструктивного синдрома: у каждого конкретного пациента тот или иной этап в эволюции бронхиальной обструкции наступает в разные сроки от начала заболевания. Это подтверждается, во-первых, ненормальностью распределения по длительности заболевания (Tзаб) в группах, а во-вторых, различной степенью альфа-стимулированной бронхоконстрикции, разным временем ее появления от начала заболевания и ненормальностью распределения по величине отрицательного ответа на адреналин в зависимости от индивидуальных особенностей субъектов, о чем говорилось выше.
Итак, результатом первой «волны» воспаления является формирование различных вариантов обструкции дыхательных путей: в одном случае с преобладанием спазма бронхов (5-я группа), а в другом — их обтурации слизистыми пробками (4-я группа). Начало новой — второй — «волны» воспаления и дальнейшее прогрессирование бронхиальной обструкции приводит к появлению выраженной альфа-стимулированной бронхоконстрикции (7-я группа) и неконтролируемой ситуации. Если предположить, что эволюция астмы происходит закономерно (см. рис. 12 — пунктирная линия), то дальнейшее прогрессирование обструкции дыхательных путей может развиваться по двум вариантам: усугубление нарушений экспекторации до III степени или усиление бронхоспазма. Во втором случае терапия стероидами и бронхолитиками эффективна, а в первом — нет. Результатом первого варианта может быть трагический исход заболевания. Подтверждением этому являются данные патологоанатомических исследований о множественной обтурации бронхов слизистыми пробками у умерших от астмы лиц (Уоннер А. Морфология обструктивных процессов в воздухоносных путях. В кн.: Бронхиальная астма. Принципы диагностики и лечения. Под ред. М.Э. Гершвина. Пер. с англ. М.: Медицина, 1984, с. 105–116).
Поэтому в таких ситуациях первостепенное значение, наряду с терапией стероидами, имеет активная эвакуация бронхиального содержимого с помощью ингаляционной отхаркивающей терапии. Результаты лечения больных свидетельствуют о том, что даже такая тяжелая ситуация теоретически может быть обратима: у субъектов аналогичной — 4-й группы ингаляционная терапия обеспечивает более эффективное очищение дыхательных путей, чем пероральная, что проявляется отсутствием альфа-стимулированной бронхоконстрикции после курса проведенного лечения и в среднем более высоким ответом на беротек.
Что касается больных с преобладанием бронхоспазма в формировании нарушения проходимости дыхательных путей и переживших вторую «волну» воспаления, то дальнейшая эволюция бронхиальной обструкции определяется у них, по-видимому, появлением третьей «волны» воспаления и по-вторением вышеописанных закономерностей.
Рассуждения о закономерной — «волнообразной» эволюции астмы не означают, что на том или ином этапе наблюдается, например, только альфа-стимулированная бронходилатация или альфа-стимулированная бронхоконстрикция. Данные проведенного исследования свидетельствуют о том, что динамика показателей ФВД и результатов фармакологического тестирования от обострения к ремиссии изменяется. Но каждый конкретный этап в эволюции бронхиальной обструкции определяется увеличением ЧАСТОТЫ тех реакций на бета- и альфа-стимуляцию, которые для него характерны.
Анализ данных обследования всех пациентов до и после лечения выявляет еще одну любопытную закономерность. Динамика показателей ФВД и ответа на фармакологические агенты от обострения к ремиссии повторяет в обратном порядке динамику этих же показателей в процессе прогрессирования астмы: возрастает величина ОФВ1 и МОС25-75, уменьшается степень спазма бронхов, исчезает тенденция к появлению альфа-стимулированной бронхоконстрикции и возрастает степень обратимости бронхиальной обструкции. Это свидетельствует о возможности обратного развития болезни с последовательным прохождением тех или иных этапов эволюции астмы.
Тот факт, что эволюция бронхиальной обструкции при астме связана в первую очередь с изменением ответа на адреналин, имеет важное биологическое значение. Именно эндогенные катехоламины (адреналин или норадреналин), являясь ЕСТЕСТВЕННЫМИ АДРЕНЕРГИЧЕСКИМИ РЕГУЛЯТОРАМИ ФУНКЦИИ ЛЕГКИХ, в начальный период заболевания оказывают бронхорасширяющее и противоотечное действие. Именно эндогенные катехоламины, циркулируя в крови, оказывают постоянное воздействие на патофизиологические механизмы астмы. И от того, насколько высока и постоянна их продукция, во многом зависит дальнейшее течение и прогноз заболевания. Что касается экзогенно поступающих в организм селективных симпатомиметиков, в частности, беротека, вентолина и пр., то именно их высокая селективность и эпизодический характер применения не позволяют воздействовать на все патофизиологические механизмы астмы и тем самым препятствовать прогрессированию бронхиальной обструкции. Что касается фармакологического тестирования, проводимого только с селективными бета-2-симпатомиметиками, то оно не позволяет в популяции одинаковых на первый взгляд субъектов выявлять все особенности формирования и эволюции бронхиальной обструкции. И это наглядно демонстрируется полученными данными: у субъектов 5, 6 и 7-й групп при одинаковой выраженности бронхиальной обструкции положительный ответ на беротек абсолютно не отражает реальной ситуации. И только последующие альфа-стимулирующие эффекты адреналина позволяют оценить и тяжесть заболевания, и его прогноз.
С учетом вышеизложенного возникает закономерный вопрос: имеют ли полученные данные какое-либо практическое значение? Ответ несомненно является положительным. Во-первых, появляется реальная возможность создания более эффективных бронходилатирующих комбинированных средств. Как видно из приведенных данных, почти у 45% обследованных субъектов отмечался положительный ответ на аль-фастимулирующее действие адреналина. Это позволило нам ранее предложить новые комбинированные препараты с более эффективным бронходилатирующим действием: бета-2-агонисты + альфа-стимуляторы; бета-2-агонисты + холинолитики + альфа-стимуляторы; холинолитики + альфа-стимуляторы (Солопов В.Н., Луничкина И.В., 1990). Организационные и финансовые проблемы не позволили запатентовать и наладить выпуск этих препаратов, однако предварительные клинические испытания были проведены. Они показали, что эффективность новых комбинированных препаратов с добавлением 0,2–0,5 мг селективных альфа-стимуляторов нафтизина и галазолина была в среднем в 1,5–2,0 раза выше, чем у обычных средств, без увеличения частоты побочных эффектов (Солопов В.Н., Луничкина И.В., 1991). По-видимому, определенная перспектива у предложенных препаратов есть. Однако при разработке, внедрении в клиническую практику и назначении этих средств следует помнить главное: АДРЕНАЛИН (как, впрочем, и другие препараты с альфа-стимулирующим эффектом) НЕ ТОЛЬКО СПАСАЕТ, НО И УБИВАЕТ!
Поскольку в эволюции бронхиальной обструкции важная роль принадлежит нарушениям экспекторации (4-я и 7-я группы), для повышения эффективности лечения представляется возможным создание комбинированных препаратов на основе пероральных стероидов и отхаркивающих средств, например: триамцинолон + бромгексин или аналогичных сочетаний. Ведь именно сочетание пероральных стероидов с отхаркивающими средствами дает возможность снизить вероятность появления альфа-стимулированной бронхоконстрикции.
Во-вторых, результаты исследования функции внешнего дыхания и фармакологического тестирования по предложенной схеме дают возможность выделить несколько вариантов бронхиальной обструкции, независимо от степени ее выраженности: а) БРОНХОСПАСТИЧЕСКИЙ (3-я и 5-я группы). У этих пациентов преобладающим механизмом обструкции является спазм бронхов. Нарушения экспекторации в 3-й и 5-й группах отсутствуют (или соответствуют 0 степени); б) ВОСПАЛИТЕЛЬНО-ОТЕЧНЫЙ (1-я и 6-я группы) — наряду с бронхоспазмом выявляется воспалительный отек слизистой. Нарушения экспекторации в 1-й группе отсутствуют, а в 6-й — соответствуют I степени; в) АЛЬФА-БРОНХОКОНСТРИКТОРНЫЙ (2-я и 7-я группы) — воспалительный отек слизистой в сочетании с нарушениями экспекторации в периферических бронхах (нарушения, по-видимому, соответствуют I-II степени) приводит к парадоксальному ответу на адреналин и г) ОБТУРАЦИОННЫЙ (4-я группа) — основным механизмом обструкции являются нарушения экспекторации, соответствующие II степени.
Выделение различных вариантов бронхиальной обструкции позволяет осуществлять дифференцированную терапию бронхорасширяющими, противовоспалительными и отхаркивающими средствами. В случае бронхоспастического и воспалительно-отечного вариантов обструкции эффективная терапия может быть обеспечена применением следующих препаратов: а) бронхорасширяющие средства — комбинация бета-2-симпатомиметиков с селективными противоотечными альфа-стимуляторами; б) противовоспалительные средства — ингаляционные стероиды и в) отхаркивающие средства в пероральной форме. В случае альфа-бронхоконстрикторного и обтурационного вариантов обструкции следует назначать другие препараты: а) бронхорасширяющие средства — комбинация бета-2-симпатомиметиков с холинолитиками; б) противовоспалительные средства — пероральные стероиды и в) отхаркивающие средства в ингаляционной форме. Эффективность проводимого лечения можно оценить по результатам повторного обследования: если в процессе динамического наблюдения данные тестирования соответствуют прохождению в обратном порядке этапов эволюции бронхиальной обструкции, то терапию можно считать эффективной. При этом основными критериями являются: возрастание показателей ФВД: ОФВ1, МОС25-75 (и других); снижение степени бронхоспазма (по ответу на беротек) с повышением обратимости бронхиальной обструкции, а также исчезновение альфа-стимулированной бронхоконстрикции (по ответу на адреналин или селективные альфа-стимуляторы).
В-третьих, появляется возможность реального клинического прогноза заболевания. Рассмотрим, например, две клинические ситуации: а) больная женщина молодого возраста с непереносимостью аспирина, не курит, принимает стероиды, бактериологический анализ мокроты выявляет наличие грамотрицательной инфекции (E. Coli); б) больной мужчина молодого возраста, курящий, без непереносимости НСПП, принимает стероиды, бактериологический анализ мокроты выявляет наличие грамположительной микробной флоры (Str. epidermidis, Str. viridans). С учетом полученных данных конечно же можно утверждать, что в первом случае прогноз заболевания хуже, чем во втором. А если при этом женщина эмоционально неустойчива, то можно предполагать, что риск внезапной смерти от астмы у нее значительно выше.
|
Каковы же первичные механизмы, являющиеся основой возникновения болезни? Об этом пойдет речь в следующей части книги.